Phân tử khối của Halothane (chính xác nhất)
Phân tử khối của Halothane hay 2-bromo-2-chloro-1,1,1-trifluoroethane (công thức phân tử là: C2HBrClF3) có phân tử khối là 197,5. Bài viết dưới đây giúp bạn hiểu rõ hơn về cách tính phân tử khối của Halothane. Mời các bạn đón đọc.
1. Halothane là gì?
- Halothane (hay 2-bromo-2-chloro-1,1,1-trifluoroethane) là một hợp chất hữu cơ, thuộc nhóm dẫn xuất halogen có công thức phân tử là C2HBrClF3.
- Halothane được sử dụng làm thuốc gây mê dạng hít trong y học.
- Halothane có phân tử khối M = 197,5.
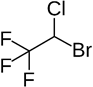
- Công thức cấu tạo của halothane:
2. Cách tính phân tử khối của halothane
- Phân tử khối của halothane: Kí hiệu là
- Cách tính phân tử khối của halothane:
= 2.MC + MH + MBr + MCl + 3.MF = 2.12 + 1 + 80 + 35,5 + 3.19 = 197,5
3. Phân tử khối là gì?
- Phân tử khối là khối lượng tương đối của một phân tử.
- Phân tử khối của một chất bằng tổng nguyên tử khối của các nguyên tử trong phân tử chất đó.
Ví dụ:
Phân tử khối của khí nitrogen (N2) bằng: 14.2 = 28.
Phân tử khối của đường (C12H22O11) bằng: 12.12 + 1.22 + 16.11 = 342.
4. Bài tập minh họa
Câu 1: Công thức phân tử của halothane là
A. CHBrClF3.
B. C2HBrClF3.
C. C2H5Cl.
D. C2HF3Cl2.
Lời giải:
Đáp án đúng là: B
Câu 2: Halothane thuộc loại hợp chất nào sau đây?
A. alkane.
B. dẫn xuất halogen.
C. carbonyl.
D. alkyne.
Lời giải:
Đáp án đúng là: B
Câu 3: Halothane có phân tử khối là
A. 78,5.
B. 109.
C. 197,5.
D. 193.
Lời giải:
Đáp án đúng là: C
Xem thêm phân tử khối của các chất hóa học hay khác:
- Phân tử khối của Allyl chloride
- Phân tử khối của Dioxin
- Phân tử khối của 2,4-dichlorophenoxyacetic acid
- Phân tử khối của CH4
- Phân tử khối của C2H6
- Phân tử khối của C3H8
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)